Современные представления о причинах злокачественной трансформации клеток - превращении их в раковые - основано на двух группах фактов.
Первая из них - существование онкогенных вирусов, или ретровирусов, содержащих РНК в качестве генетического материала, ДНК-копии которых могут встраиваться в геном инфицируемой клетки (см. гл. 10). Результатом этого процесса может быть злокачественное новообразование. Онкогенные вирусы содержат онкоген, экспрессия которого и ответственна за канцерогенез. Этот механизм восходит к вирусо-генетической теории рака, предложенной в 1945 г. советским ученым Л. А. Зильбером.
Вторая группа фактов сводится к тому, что разнообразные внешние воздействия на клетки, в большинстве случаев (но не всегда) мутагенные, также могут привести к их превращению в раковые. Наследственные заболевания человека, связанные с нарушениями репарации (см. гл. 20), сопровождаются повышением мутабильности соматических клеток, судя по хромосомным аберрациям, и тоже характеризуются повышенной частотой злокачественных новообразований. Предположения о мутационной природе канцерогенеза высказываются с начала XX в., начиная с работы Т. Бовери (1914).
Таким образом, первая группа фактов побуждает искать причину рака в действии генетического материала, вносимого в клетку извне, а вторая - искать генетические причины рака в самой клетке. Эти подходы объединяют сведения о том, что в нормальных клетках существуют так называемые протоонкогены - гены, гомологичные онкогенам ретровирусов. Протоонкогены чрезвычайно консервативны и сходны в геномах человека, мыши, дрозофилы и даже дрожжей. Некоторые из них контролируют нормальное протекание клеточного цикла. Нельзя сказать, что механизм канцерогенеза выяснен, однако наиболее вероятной причиной представляется злокачественная трансформация клетки вследствие нарушения экспрессии некоторых ее генов (онкогенов, протоонкогенов) в результате мутационных или модификаци- о иных изменений, а также в результате вирусной инфекции.
В свете этих представлений распространение в окружающей среде генетически активных агентов может приводить не только к повышению частоты мутаций, но и к повышению частоты злокачественных новообразований. В связи с этим программы тестирования химических соединений различных физических и биологических факторов предусматривают выявление среди них потенциальных канцерогенов. Учитывая важность этой задачи, в международном масштабе разрабатываются чувствительные тест-системы выявления канцерогенов, координируемые Всемирной организацией здравоохранения и другими международными организациями. В частности, для выявления канцерогенов используются кратковременные тесты, перечисленные в табл. 21.3, дополненные прямым испытанием химических соединений на их способность вызывать злокачественную трансформацию в культурах клеток животных и человека, а также у животных (мыши, крысы, хомяки). При высоком уровне корреляции (до 90 %) мутагенных и канцерогенных свойств химических препаратов определенные трудности
возникают в связи с тем, что некоторые канцерогены генетически неактивны, а некоторые активные мутагены не являются канцерогенами. Дальнейшее совершенствование систем тестирования мутагенов и канцерогенов должно способствовать не только обеспечению генетической безопасности человека, но и пониманию механизмов канцерогенеза.
Все мероприятия по выявлению генетически активных факторов направлены на сведение к минимуму контактов человека с мутагенами. Новые химические соединения и другие генетически активные агенты изымаются из употребления или их применение строго ограничивается. В тех же случаях, когда человек вынужден с ними соприкасаться, необходимо иметь в резерве средства минимизации риска мутационных и канцерогенных изменений. Для этого необходимо знать пути мутагенеза и уметь вмешиваться в этот процесс. Становление мутации - процесс многоэтапный. В упрощенном виде его можно представить так, как это показано на схеме рис. 21.5. Многие мутагены, попадая в организм, включаются в цепи метаболических превращений и затем могут как активироваться, т. е. приобрести или повысить свою генетическую активность, так и инактивироваться, т. е. потерять ее. При этом необходимо учитывать организменные и клеточные барьеры проницаемости и способ попадания соединения в организм: через кожу; дыхательные пути и т. д.
Оказавшись внутри клетки, мутаген взаимодействует с генетическим материалом - с хроматином или непосредственно с ДНК ядра или клеточных органелл. В результате такого взаимодействия в ДНК возникают первичные изменения, которые по мнению одних авторов можно считать пред мутационными, а по мнению других эти изменения должны превратиться в предмутационные на следующем этапе.
Большинство предмутационных изменений устраняется системами репарации (см. гл. 6.12): конститутивная безошибочная репарация восстанавливает исходную структуру молекулы ДНК, а индуцибельная репарация, склонная к ошибкам, может фиксировать мутационные изменения. Фиксация мутации сопровождается ее фенотипическим проявлением, если мутация доминантна или если она находится в гомозиготе, будучи рецессивной, в отсутствие эпистатирующих генов или супрессоров в условиях, не вызывающих фенокопии нормы. Каждый из рассмотренных этапов может быть разбит на более дробные стадии.
В ряде случаев есть возможность вмешаться в процесс становления и проявления мутации. Если начать с последнего этапа - проявления мутации, то фе но копирование нормы - задача медицины и медицинской генетики, которые способны предотвращать развитие болезни во многих случаях наследственных патологий (гл. 20).
Рис. 21.5. Последовательные этапы возникновения и проявления мутаций. Пояснения в тексте
Развиваются исследования по антимутагенезу. Это понятие включает такие воздействия на клетку и организм, которые блокируют или уменьшают вероятность возникновения мутаций. Подобные воздействия могут стимулировать системы инактивации мутагенов или подавлять системы активации промутагенов, могут стимулировать процессы безошибочной репарации или непосредственно модифицировать мутаген, «отвлекать» его от генетического материала (рис. 21.5).
Антимутагепной активностью обладают радиопротекторы - соединения, способные уменьшать летальный эффект ионизирующей радиации, прежде всего серосодержащие аминокислоты: цистеин, I(истин, метионин и др.
Обычно для каждого конкретною мутагена антимутагенная активность специфична, что затрудняет поиски антимутагенов. Генетическую активность!\!"-мети ч- N"-ниrpo- N"-нитрозогуанидина
(МННГ) нейтрализует кровь млекопитающих, в которой основным антимутагеном (анти-МННГ) служит гемин. Ненасыщенные жирные кислоты, тониновая кислота и катехин, содержащийся в чае и кофе, некоторые витамины, например а-токоферол, и другие соединения обладают большей или меньшей антимутагенной активностью по отношению к отдельным мутагенам.
К сожалению, разнообразие исследованных соединений и объектов так велико, что не представляется возможным делать какие- либо обобщения о природе антимутагенных эффектов. Кроме того, исследователи обычно не могут контролировать различные этапы становления мутации (рис. 21.5). Отсутствуют тест-системы, специализированные для поиска антимутагенов.
Обращаясь к проблеме уменьшения генетической опасности, следует помнить, что человеческие популяции гетерогенны по многим признакам (см. гл. 20), в том числе по реакции на различные воздействия внешних факторов. Это обстоятельство уже учитывает фармако генетика, изучающая реакцию различных групп людей на лекарственные вещества. Известно, например, что у некоторых больных сульфаниламидные препараты вызывают гемолиз. Это связано с наследственной недостаточностью глю- козо-6-фосфатдегидрогеназы. Есть категория людей с наследственной болезненной реакцией на глюкокортикоиды. При применении этих препаратов у них повышается внутриглазное давление. Нестабильность некоторых мутантных форм гемоглобина сопряжена с гемолизом при применении окислителей.
Известна также наследственная чувстительность к действию некоторых мутагенов и канцерогенов. Например, люди с повышенной активностью арилгидрокарбонгидроксилазы склонны к заболеваниям раком легких в случае контакта с полициклическими углеводородами, которые после гидроксилирования указанным ферментом превращаются в эпоксиды, обладающие высокой канцерогенной активностью.
Эти обстоятельства необходимо учитывать в разных областях человеческой деятельности: при лечении больных, при профессиональном отборе людей, имеющих дело с различными производственными вредностями.
Итак, меры по обеспечению генетической безопасности человека связаны с решением многих проблем, обших для генетики и экологии, и прежде всего охраны окружающей среды от загрязнения. Генетическая токсикология делает при этом главный акцент на генетически активные факторы. Эта работа, начавшаяся в 60-х годах в связи с ростом темпов научно-технической революции, стала неотъемлемой частью и условием дальнейшего прогресса технологии во всех областях промышленности и сельского хозяйства. Генетическая безопасность человечества должна основываться и на знании популяционной генетики человека, учитывающей полиморфизм человеческих популяций, предрасположенность людей к отрицательным реакциям на различные факторы окружающей природной и производственной среды. При
выявлении мутагенной и канцерогенной активности многих веществ, используемых ныне в сельском хозяйстве, необходима большая осторожность в их применении. Перспектива отказа от использования этих генетически активных веществ связана с разработкой биологических методов борьбы с сорняками, насекомыми-вредителями и т. д. Учет этой перспективы, а также необходимость дальнейшей селекции полезных человеку организмов невозможны без бережного отношения к биологическим природным ресурсам. Особого внимания в этом деле заслуживает сохранение генофонда планеты, который представляет собой постоянный источник полезных форм, а теперь является источником конкретных генов, которые могут быть использованы для создания новых сортов растений, пород животных и штаммов микроорганизмов.
Мутагенез – процесс образования мутаций. Факторы, вызывающие мутации – это мутагены. Мутагены воздействуют на генетический материал особи, вследствие чего может измениться фенотип.
Канцерогенез – процесс образования опухолей. Установлено, что при канцерогенезе изменения происходят на молекулярно-генетическом уровне и затрагивают механизмы, отвечающие за размножение, рост и дифференцировку клеток.
Классификации мутаций.
По причинам, вызвавшим мутации:
Спонтанные (самопроизвольные). Происходят по действием естественных мутагенных факторов без вмешательства человека.
Индуцированные. Результат направленного воздействия определенных мутагенных факторов.
По мутировавшим клеткам:
Генеративные. Происходят в половых клетках. Передаются по наследству.
Соматические. Происходят в соматических клетках. По наследству передаются только при вегетативном размножении.
По исходу для организма:
Летальные. Несовместимые с жизнью.
Полулетальные. Снижают жизнеспособность организма.
Нейтральные. Не влияют на процессы жизнедеятельности.
Положительные. Повышающие жизнеспособность. Возникают редко, но имеют большое значение для прогрессивной эволюции.
По изменениям генетического материала:
Геномные. Обусловлены изменениями числа хромосом. Обнаруживаются цитогенетическими методами. Всегда проявляются фенотипически.
Полиплоидия (кратное гаплоидному увеличение числа хромосом (3n, 4n, 5n), имеет большое значение для селекции., гаплоидия). У млекопитающих и человека – это летальные мутации
Гаплоидия (1n). Н-р, трутни у пчел. Жизнеспособность снижается. В данном случает проявляются все рецессивные гены. Для млекопитающих и человека мутация летальна.
Анеуплоидия. Некратное гаплоидному уменьшение или увеличение числа хромосом (2n+\-1). Разновидности:
Трисомия. 2n + 1. В генотипе 3 гомологичные хромосомы. Болезнь Дауна
Моносомия. В наборе одна из пары гомологичных хромосом. 2n – 1. Моносомия по первым крупным парам хромосом для человека летальна.
Нулесомия. Отсутствие пары хромосом. Летальная мутация.
Хромосомные (оберации). Обусловлены изменением структуры хромосом. Могут быть внутри и межхромосомными. Выявляются цитогенетичесмкими методами.
Внутрихромосные. Перестройки внтури хромосом
Межхромосомные. Происходят между негомологичными хромосомами. Транслакация, дубпликации.
Генные (точечковые, трансгенации). Связаны с изменениями структуры гена (молекулы ДНК). В большинстве случаев проявляются фенотипически. Являются причиной нарушения обмена веществ, генных болезеней. Частота проявления – 1-2%. Выявляются биохимическими методами и методами рекомбинантной ДНК.
Изменения структурных генов. Сдвиг рамки считывания. Приводит к миссенс-мутациям (изменению смысла кодонов и образованию других белков). Нонсенс-мутации – образование бессмысленных кодонов, не кодирующих аминокислоты.
Изменения функциональных генов.
Белок репрессор не подходит к гену-оператору. Структурные гены работают постоянно. Белки синтезируются все время
Белок-репрессор не снимается индуктором. Структурные гены постоянно не работают. Синтеза белка нет.
Нарушение чередований репрессий и индукций.
Лекция 3. УД «Генетика человека с основами медицинской генетики» по теме «Мутации и мутагенные факторы»
Цель лекции:
Изучение закономерностей мутагенеза
Изучение причин мутаций
Изучение значения понятия «генетический груз»
Изучение классификации мутагенов
Ознакомление с терминологией генетики
План лекции:
Мутагенез.Понятие о мутагенах. Классификация мутагенов.Виды мутаций. Классификация мутаций.
Изменчивость - свойство организмов приобретать новые признаки и особенности индивидуального развития под влиянием среды. Различают модификационную и генотипическую изменчивость.
Модификационная изменчивость - это способность организма реагировать на условия окружающей среды, изменяться в пределах нормы реакции организма.
Наследственная изменчивость - это способность к изменению самого генетического материала.
При всех формах изменчивости имеется генетический контроль и о происшедших изменениях можно судить лишь по фенотипу (по изменению признаков и свойств организма).
Модификации развиваются в естественных условиях среды и подвергаются действию факторов, много раз встречавшихся в процессе филогенеза, то есть норма реакции складывалась исторически.
Модификации, напоминающие проявления мутаций известных генов, называются фенокопии. Они сходны с мутациями, но механизм их возникновения различен (катаракта может быть следствием как мутации, так и фенокопией).
Модификации имеют приспособительное значение и способствуют адаптации организма к условиям окружающей среды, сохраняют гомеостаз организма.
Изучение модификационной изменчивости проводится с помощью близнецового метода (соотносительная роль наследственности и среды в развитии признака) и метода вариационной статистики (изучение количественных признаков).
Генотипическая изменчивость связана с качественными и количественными изменениями наследственного материала. Она включает комбинативную и мутационную изменчивость.
1. Комбинативная изменчивость. Уникальность каждого генотипа обусловлена комбинативной изменчивостью, которая определяется новыми сочетаниями аллелей генов в генотипе. Достигается это в результате 3-х процессов: два из них связаны с мейозом, третий - с оплодотворением.
2. Мутационная изменчивость. При мутационной изменчивости нарушается структура генотипа, что вызвано мутациями. Мутации - это качественные, внезапные, устойчивые изменения в генотипе.
Существуют различные классификации мутаций.
По уровню изменения наследственного материала (генные, хромосомные, геномные);
По проявлению в фенотипе (морфологические, биохимические, физиологические);
По происхождению (спонтанные, индуцированные);
По их влиянию на жизнь организма (летальные, полулетальные, условно летальные);
По типам клеток (соматические и генеративные);
По локализации в клетке (ядерные, цитоплазматические).
Генные мутации связаны с молекулой ДНК - нарушение нормальной последовательности нуклеотидов, свойственной данному гену. Это может быть вызвано изменением количества нуклеотидов (выпадением или вставкой) или их заменой.
Мутации появляются в генотипе с определённой частотой и часто проявляются фенотипически. Некоторые из них являются причиной возникновения генных (молекулярных) болезней. В организме имеются механизмы, ограничивающие неблагоприятный эффект мутаций: репарация ДНК, диплоидный набор хромосом, вырожденность генетического кода, повтор (амплификация) некоторых генов.
Хромосомные мутации (аберрации) заключаются в изменении структуры хромосом (внутрихромосомные и межхромосомные).
Внутрихромосомные мутации: делеции, дупликации, инверсии. При делециях и дупликациях изменяется количество генетического материала, а при инверсиях - его расположение. При межхромосомных мутациях происходит транслокация наследственного материала, обмен участками между негомологичными хромосомами.
Геномные мутации заключаются в изменении числа отдельных хромосом (гетероплоидия) или нарушении геномного числа хромосом (полиплоидия).
Хромосомные и геномные мутации являются причинами хромосомных болезней. Разработана система обозначений мутаций (Денверская и Парижская классификация).
Мутации имеют значение в онто- и филогенезе, они приводят к появлению новых свойств наследственного материала: генные - появлению новых аллелей, хромосомные аберрации - к образованию новых групп сцепления генов, геномные мутации - новых генотипов. Они обеспечивают фенотипическое разнообразие организмов.
Мутагенез (мутационный процесс)
Мутационный процесс - процесс возникновения, формирования и реализации наследственных нарушений. Основой мутационного процесса являются мутации. Мутации происходят как в естественной среде обитания организмов, так и в условиях направленного воздействия мутагенами. В зависимости от этого различают спонтанный и индуцированный мутагенез.
Спонтанный мутагенез - это самопроизвольный процесс возникновения мутаций под влиянием естественных факторов среды. Существует несколько гипотез относительно генеза спонтанных мутаций: естественная радиация, наличие генов-мутаторов, определенное соотношение мутагенов и антимутагенов и др.По современным данным мутации возникают при нарушении процесса репликации и репарации ДНК.
Спонтанный мутационный процесс характеризуется определенной интенсивностью (частотой генных, хромосомных и геномных мутаций), непрерывностью, ненаправленностью, отсутствием специфичности; он является одной из биологических характеристик вида (стабильность генотипа) и протекает постоянно. Частота спонтанных мутаций подвергается генному контролю (ферменты репарации) и параллельно влиянию естественного отбора (появление новых мутаций уравновешивается их элиминацией). Познание закономерностей спонтанного мутагенеза, причин его возникновения необходимо для создания специальных методов слежения за мутациями, чтобы контролировать их количество у человека.
Индуцированный мутагенез - возникновение мутаций под влиянием направленных специальных факторов внешней среды - мутагенов.
Способностью индуцировать мутации обладают различные мутагены физической, химической и биологической природы, которые вызывают соответственно радиационный, химический и биологический мутагенез.
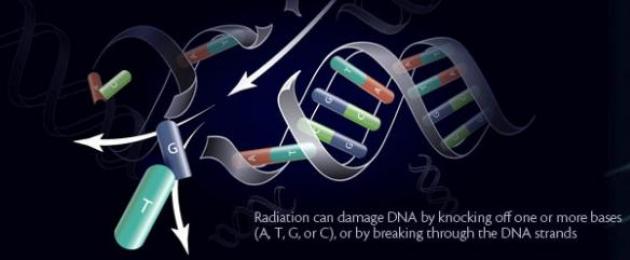
Физические мутагены: ионизирующее излучение, ультрафиолет, температура и др. Ионизирующая радиация оказывает непосредственное действие на гены (разрыв водородных связей ДНК, изменение нуклеотидов), хромосомы (хромосомные аберрации) и геномы (изменение числа и наборов хромосом). Эффект радиации сводится к ионизации и образованию свободных радикалов. Разные формы живых организмов характеризуются различной чувствительностью к радиации.
Химические мутагены (лекарственные препараты, никотин, алкоголь, гербициды, пестициды, кислоты, соли и др.) вызывают генные, реже хромосомные мутации. Мутагенный эффект больше у тех соединений, которые способны взаимодействовать с ДНК в период репликации.
Биологические мутагены (вирусы, живые вакцины и др.) вызывают генные мутации и хромосомные перестройки. Мутагенный эффект избирателен в отношении отдельных генов.
При оценке индуцированных мутаций учитывают индивидуальный и популяционный прогноз. Все виды мутагенеза опасны при вовлечении больших популяций людей.
Для защиты живых организмов от поражающего действия мутагенов используются антимутагены, организуется комплексная система генетического мониторинга и химического скрининга.
Репарация генетического материала
ДНК отличается высокой стабильностью, которая поддерживается особой ферментативной системой, находящейся под генетическим контролем, она же принимает участие и в репарации. Многие повреждения ДНК, которые могли бы реализоваться в виде мутаций при действии сильных мутагенов, исправляются репаративными системами.
Генетические различия в активности репарирующих ферментов определяют разную продолжительность жизни и устойчивость организмов к действию мутагенов и канцерогенов. У человека некоторые болезни (прогерия) связаны с нарушением процесса репликации и репарации ДНК. Моделью для изучения генетических механизмов репарации является заболевание –пигментная ксеродерма. Известно, что 90% мутагенов являются и канцерогенами. Существует несколько теоретических концепций (теорий) канцерогенеза: мутационная, вирусно-генетическая, концепция онкогена и др.
Генетический мониторинг
Человек контактирует с разнообразными химическими веществами, проверить каждое на возможность мутагенного (канцерогенного) эффекта или генотоксичности не представляется возможным, поэтому проводится отбор определенных химических веществ для исследования на мутагенность.
Выбор того или иного вещества определяется:
Его распространением в среде обитания человека и контактом с ними большей части населения (лекарства, косметические средства,
продукты питания, пестиды и др.)
Структурным сходством с известными мутагенами и канцерогенами (нитрозосоединения, ароматические углеводороды) Для исследования на мутагенность
Используется несколько тест-систем (около 20 из 100 имеющихся методов) т.к. нет универсального теста для выявления всех типов мутаций в половых и соматических клетках.
Применяется ступенчатость тестирования (в начале на микроорганизмах, дрозофиле и др. объектах и только потом в клетках человека.)
Иногда достаточно использование одной тест-системы, для выявления мутагенности вещества и соответственно невозможность его использования.
Генетический мониторинг - это система долговременных популяционных исследований по контролю за мутационным процессом у человека (слежение за мутациями). Он складывается из:
Химического скрининга - экспериментальной проверки мутагенности химических соединений (слежение за мутациями в тест-системах)
Прямого анализа частот генных мутаций
Феногенетического мониторинга.
Система тестирования состоит из просеивающей и полной программы, возможность их использования определяется степенью контакта населения с данным химическим веществом.
Мутация всегда происходит внезапно. Генетический материал организма изменяется: что-то происходит внутри хромосом или генов, и эти перемены обычно видны невооруженным глазом. В некоторых случаях последствия тяжелы, а иногда для организма возможен Мутация не возникает сама по себе. Причиной всегда становится мутагенный фактор.
Что такое мутагенные факторы?
Изменения, происходящие в генах и хромосомах, изучает наука генетика. Она же и дает научное определение мутагенам.
Мутагенные факторы - это химические или физические агенты, вызывающие изменения генетического материала клетки. Природа этих агентов может быть различной, на этом положении и основывается их классификация.
Виды мутагенов
В зависимости от их происхождения выделяют физические, химические и биологические мутагены. Любой мутагенный фактор можно отнести к одной из этих трех основных групп.
Воздействие враждебных клетке агентов может быть направлено непосредственно на ДНК, и тогда молекула генетического материала теряет исходную структуру. Некоторые мутагены вмешиваются в процесс деления клетки, и в результате наследственный материал распределяется неправильно. Существуют, однако, и вещества, которые сами по себе к мутагенам отнести нельзя. Но воздействие на такое химическое соединение определенных ферментов превращает его в самый настоящий мутагенный фактор. Эти вещества, имеющие мутагенный «потенциал», называют промутагенами.
Мутагенные факторы. Примеры
К мутагенам физического происхождения можно отнести источники воздействие ультрафиолета, аномально высокие или низкие температуры, влажность.

К примеру, волны ультрафиолетового излучения, имеющие длину свыше 260 нм, поглощаются клеткой листа растения и вызывают образование в ней нехарактерных пиримидиновых димеров (соединений в цепи ДНК), которые, в свою очередь, становятся причиной ошибок в считывании генетического материала. В результате новые клетки получают с «неправильной» структурой.
Многие химические вещества относятся к мутагенам и промутагенам. Примерами могут служить активные формы кислорода, нитраты и нитриты, некоторые металлы, лекарства и те вещества, которых до появления человечества в природе не существовало (бытовая химия, пищевые добавки и консерванты).
К примеру, беременная женщина может не знать о своем положении и принимать некоторые антибиотики, опасные для плода. В результате у ребенка могут развиться вызванные мутациями.
Результатом воздействия таких биологических агентов на клетку является процесс, который называется инфекционным мутагенезом. К примеру, бактерия Helicobacter pylori, живущая в кишечнике и желудке человека, может вызывать воспалительные процессы на слизистой. Воспаление изменяет нормальный ход окислительно-восстановительных процессов в поврежденных клетках, что меняет и структуру генетического материала в них. Нарушаются процессы восстановления ДНК и ход нормального деления молекулы. Результат - мутации.

Несколько слов о процессе мутагенеза
Мутагенез - это сам процесс возникновения мутации. Какими же механизмами он может происходить?
Самые сильные мутагенные факторы вызывают так называемую хромосомную нестабильность. В результате генетический материал либо распределяется в разделившихся клетках неравномерно, либо изменяется сама структура хромосомы. К примеру, две хромосомы под воздействием агрессивного агента обмениваются своими участками.
Мутагенный фактор может также изменить последовательность нуклеиновых кислот ДНК. Интересно, оказываются летальными или являются причиной очень серьезных заболеваний, когда затронуты важные нуклеотиды, но могут они происходить и без патологий, если такие последовательности нуклеиновых кислот не повреждаются.
Как защитить себя от воздействия мутагенов?
Мутагенные факторы не вездесущи, поэтому предпринять определенные меры профилактики все же будет полезно.
Антиоксиданты - важная группа соединений, препятствующих воздействию канцерогенов. Они могут помочь и защититься от разного рода враждебных химических агентов. Примерами антиоксидантов являются витамины А, В и Е, бета-каротины и флавоноиды. Эти вещества в очень большом количестве содержатся в овощах и фруктах, а также в зеленом чае.
Важно стараться защищать себя от воздействия неблагоприятных физических агентов, таких как УФ-излучение или табачный дым. К примеру, в Австралии проживает очень большое количество светлокожих людей, и там часто стоит солнечная погода. Процент заболевших меланомой в этой стране, к сожалению, высок.
С осторожностью нужно принимать антибиотики, внимательно относиться к продуктам питания и стараться свести к минимуму потребление консервантов. Идеально, конечно же, было бы придерживаться принципов здорового питания.
Мутагенные факторы среды сильны. Однако защитить себя от их воздействия вполне реально, если внимательно относиться к своему здоровью.
Предположим, что мутагенный фактор вызвал нарушение в гене-репрессоре 1 и активный репрессор 1 не может быть синтезирован. В этом случае растормаживается ген инициатора клеточного деления и начинается репликация ДНК.
Образовавшиеся в результате деления клетки не располагают геном-репрессором 1, вследствие чего клетки продолжают репликацию ДНК и при делении образуется семейство клеток, способных к беспредельному неконтролируемому делению. Очевидно, они и являются опухолевыми клетками.
Аналогичным образом к беспредельному клеточному делению могут привести мутации и других генов данной регуляторной системы, например мутация гена, кодирующего инициатор клеточного деления, в результате которой он становится недоступным тормозящему влиянию гена-репрессора 1.
Наряду с мутационным возможен и эпигеномный канцерогенез, который предполагает приобретение здоровой клеткой опухолевых свойств путем воздействия на геном клетки факторов, которые не принадлежат к геному данной клетки и не вызывают мутацию, но создают устойчивое нарушение нормальной регуляции генома, приводящее к беспредельному росту
Передающееся из поколения в поколение эпигеномное влияние может сформироваться, например, под действием вируса, инфицирующего исходную и попадающего в каждую новообразовавшуюся клетку в митозе (рис. 13.3). Допускается, что в геноме вируса имеется ген типа клеточного гена-репрессора. 2. C появлением вируса в клетке начинается синтез вирусного репрессора 2, который тормозит работу гена-репрессора 1, и репрессор 1 не синтезируется. В отсутствие репрессора 1 активизируется. ген, кодирующий инициатор деления клетки, и синтезируется данный инициатор. Появление инициатора деления клетки приводит к началу репликации ДНК, имеющейся в геноме клетки, т. е. к делению клетки. При этом инициатор деления выключает ген-репрессор 2 клетки, но не может выключить онкогенную часть генома вируса - вирусный ген-репрессор типа клеточного гена-репрессора 2 в силу особенностей строения вирусного гена-репрессора 2. Таким образом, пока вирус находится в клетке, постоянно поддерживается синтез репрессора 2 на основе вирусного гена. Это приводит к репрессии регуляторного гена-репрессора 1 клетки, в связи с чем дерепрессируется ген, кодирующий инициатор деления клетки и клетка продолжает размножаться.
Образовавшиеся клетки содержат в себе вирусный геном, который попадает к ним во время митоза от исходной клетки и поддерживает нарушение регуляции клеточного деления в последующих поколениях клеток. Получены доказательства, что онкогены опухолеродных вирусов действительно идентичны клеточным факторам роста. Более того, в клетках сетчатки найден ген-репрессор клеточного деления, названный Rb, наследственный дефект которого приводит у ребенка к развитию злокачественной опухоли сетчатки глаза - ретинобластомы.
Мутационный и эпигеномный механизмы канцерогенеза не исключают друг друга, а могут быть сопряженными. В клетке имеются специальные регуляторные гены, репрессирующие геном опухолеродного вируса (см. рис. 13.1). Следовательно, мутация может произойти с репрессорным геном клетки, в результате чего активируется вышедший из-под контроля онкоген опухолеродного вируса и происходит эпигеномная трансформация клетки. Таким образом, химические и физические факторы могут не сами по себе вызывать трансформацию, а способствовать активизации вирусного канцерогенеза.
Рис. ІЗЛ. Модель контроля онко- и вирусогенеза.
Опыты Гердона по пересадке ядер дифференцированных клеток в цитоплазму зиготы были использованы для изучения регуляции деления в ядрах опухолевых клеток. Если из оплодотворенных яйцеклеток лягушки удаляют ядро и вместо него подсаживают ядро из специализированной клетки с двойным набором хромосом, например клетки кишечного эпителия, то развивается головастик со всеми дифференцирующимися органами. Следовательно, в ядрах специализированных клеток организма сохраняется весь набор генов, который был в ядре зиготы. Когда в цитоплазму зиготы подсадили ядро раковой клетки из почечной опухоли Люкке лягушки, также развился головастик, а не опухолевая ткань. После пересадки ядра клетки такого головастика в цитоплазму клетки опухоли Люкке образовалась нормальная почечная ткань.
Таким образом, здоровая цитоплазма зиготы обусловила полное восстановление регуляции в пересаженном ядре опухолевой клетки и закрепление его как наследуемое свойство. Поскольку опухоль Люкке лягушек имеет вирусное происхождение, следовательно, речь идет о восстановлении функции генов, репрессирующих вирусный геном.