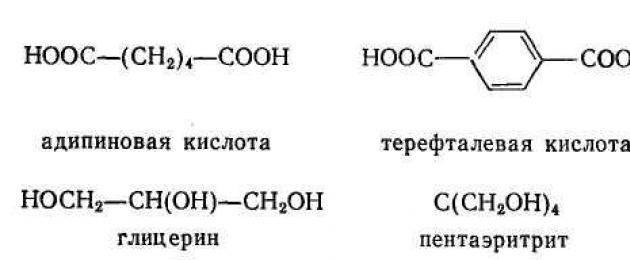Катализ в нефтехимии
Общие сведения о каталитических методах переработки нефти и нефтяных углеводородов. Основные типы гетерогенных катализаторов в нефтехимических процессах.Специфические особенности разных областей катализа: гомогенного, гетерогенного и микрогетерогенного. Активные центры. Характеристики катализаторов – активность, селективность. Энергетические аспекты в катализе. Электронные факторы в гетерогенном катализе. Промоторы и яды. Стадии адсорбции и диффузии в гетерогенном катализе. Макрокинетические факторы в катализе. Кислотно-основной катализ. Гомогенный катализ, металлокомплексный катализ. Координация и лигандный обмен. Каталитические циклы. Ключевые реакции в гомогенном катализе. Окислительное присоединение и восстановительное элиминирование. Реакции внедрения. Катализ ионами и комплексами. Ферментативный катализ.
Новые подходы к иммобилизации катализаторов. Двухфазный катализ (SHOP –процесс получения альфа-олефинов). Водорастворимые металлокомплексные катализаторы (процесс гидроформилирования пропена и бутена-1 фирмы Rhone-Poulenc/Ruchrchemie). Фторный катализ. Металлокомплексный катализ в сверхкритическом диоксиде углерода. Катализ в ионных жидкостях.
Использование синтетических рецепторов в катализе. Супрамолекулярные катализаторы. Способность к молекулярному узнаванию и субстратная селективность
Проблемы дезактивации и регенерации катализаторов.
Кинетические методы исследования реакций и катализаторов. Моделирование процессов. Методы оптимизации процессов.
Получение первичных нефтехимических продуктов на базе вторичных процессов переработки нефти
Процесс пиролиза – источник нефтехимических продуктов: этилена, пропилена, бутиленов, дивинила, изопрена, аллена, ароматических углеводородов. Сырье для пиролиза.
Каталитический крекинг, сырье для крекинга. Катализаторы крекинга – аморфные алюмосиликаты, цеолиты и др., их стабильность. Отравление катализаторов металлами, содержащимися в тяжелых нефтяных фракциях и остатках. Пассивация каталитического действия металлов, пассиваторы. Механизм каталитического крекинга. Поведение углеводородов различных классов в условиях каталитического крекинга.
Основные продукты каталитического крекинга. Гидрокрекинг. Роль водорода в процессе. Гидроочистка.
Ресурсы ароматических углеводородов. Выделение ароматических углеводородов. Бензол и пути его использования. Способы увеличения ресурсов бензола. Ксилолы, ресурсы, разделение изомеров. Пути увеличения ресурсов п-ксилола. Кумол, синтез и окисление.
Химия кислород- и серосодержащих составляющих продуктов переработки нефти и угля
Фенолы. Источники фенолов, способы выделения и разделения. Способы получения одно-, двух- и многоатомных фенолов. Затрудненные фенолы. Таутомерия фенолов. Реакции электрофильного замещения в ряду затрудненных фенолов. Бисфенолы. Антиокислительные свойства фенолов. Фенолы – присадки к топливам, маслам и полимерным материалам.
Сероорганические соединения нефтей в нефтехимии. Современное состояние проблемы утилизации органических соединений серы нефтей, ее химические, экологические и экономические аспекты. Особенности химического поведения нефтяных сероорганических соединений. Практическое использование нефтяных сернистых концентратов. Применение нефтяных меркаптанов, сульфидов, тиофенов. Использование нефтяных дисульфидов вторичного происхождения.
Экономический эффект использования нефтяных органических соединений серы (на примере нефтяных сернистых экстрагентов).
Получение органических производных серы на базе нефтехимического сырья.
Каталитический синтез меркаптанов. Метилмеркаптан, метионин, додецилмеркаптаны.
Производство диметилсульфида.
Производство сульфоксидов и сульфонов. Диметилсульфоксид. Сульфолан. Дивинилсульфоксид.
Производство тиофенов, бензотиофена. Области применения этих соединений.
Перспективные пути производства органических соединений серы.
Синтезы на базе ацетилена. Высокотемпературные реакции органических соединений с сероводородом, тиолами, сульфидами, дисульфидами, сульфоксидами. Новые каталитические синтезы. Органические соединения серы, содержащие другие гетероатомы.
Альтернативное сырье для нефтехимического синтеза
Уголь – альтернатива нефти и природному газу как сырью нефтехимической промышленности.Методы переработки углей в углеводородное сырье (термическое растворение, гидроожижение, деструктивное гидрирование).
Газификация углей. Полукоксование и коксование. Коксовая смола – источник ароматического сырья.
Использование оксида и диоксида углерода в производстве топлив и нефтехимического сырья. Процесс Фишера-Тропша. Современные представления о механизме.
Метанол – топливо и сырье для нефтехимического синтеза. Превращение метанола в углеводороды. Простые метиловые эфиры – неуглеводородные добавки к топливу.
Использование оксида и диоксида углерода в синтезе органических веществ различных классов.
Литература
1.Л.Пакетт. Основы современной химии гетероциклических соединений. М.: Мир, 1971.
2.Т.Джилкрист, Р.Старр.Органические реакции и орбитальная симметрия. М.:Мир, 1986.
3.Karakhanov E.A., Maksimov A.L. Catalysis by soluble Macromolecular Metal
Complexes. In. Editors Wohrle E.D., Pomogailo A.D. Metal Complexes and Metals in
Macromolecules. Synthesis, Structure and properties. 2003, Wiley-VCH [email protected] . P.457-502.
4.Н.К.Ляпина. Химия и физикохимия сераорганических соединений нефтяных дистиллятов. М.: Наука, 1984.
5.В.Ф.Камьянов, В.С.Аксенов, В.И.Титов. Гетероатомные компоненты нефтей. Новисибирск: Наука, 1984.
6.Н.С.Печуро, Д.В.Панин, О.Ю.Песин.Химия и технология синтетического топлива и газа. М.: Химия, 1986.
7.Р.А.Шелдон. Химические продукты на основе синтез-газа. М.: Химия, 1987.
8.Г.Хенрицци-Оливэ, С.Оливэ. Химия каталитического гидрирования СО. М.: Химия, 1987.
9.Катализ в С1-химии (под ред.Клайма Л.) Ленинград: Химия, 1987.
10.В.С. Арутюнов, О.В. Крылов.Окислительные превращения метана. М.: Наука, 1998.
Основным углеводородным сырьем для нефтехимических синтезов являются смеси газообразных, жидких и твердых углеводородов.
Природные газы состоят в основном из метана и других насыщенных углеводородов; в них также присутствуют инертные газы (азот, диоксид углерода) и редкие газы (аргон, ксенон). Природные газы добывают при разработке газовых и конденсатных месторождений.
Попутные нефтяные газы получают как побочный продукт при добыче нефти. Эти газы растворены в пластовой нефти и при ее добыче выделяются вследствие снижения давления. Попутный нефтяной газ состоит из насыщенных углеводородов от метана до пентанов и обычно содержит некоторое количество инертных газов; попутные газы некоторых месторождений содержат также свободный сероводород. Как правило, попутные нефтяные газы содержат значительные количества углеводородных компонентов – этана, пропана и бутанов, являющихся ценным сырьем для нефтехимии.
Газы нефтепереработки образуются в процессах крекинга, коксования, риформинга; их также отбирают на установках стабилизации и прямой перегонки нефти. В зависимости от характера этих процессов состав получаемых газов меняется в широких пределах. Например, газы каталитического риформинга содержит до 60% водорода; остальное – насыщенные углеводороды. Газы крекинга и коксования состоят из насыщенных и ненасыщенных углеводородов.
Газы стабилизации нефти отличаются высоким содержанием пропана, бутана, пентана и изопентана, что делает их ценным сырьем для получения бутадиена и изопрена.
Газовые бензины выкипают в интервале 30-120 0 С; они содержат бутан, пентан, изопентан, а также углеводороды С 6 и С 7 нормального строения и изостроения.
Газовые конденсаты выкипают в интервале 40-360 0 С. В них содержится 15-30% ароматических углеводородов; 25-40% нафтенов и 20-60% парафинов (в зависимости от месторождения).
Жидкие дистилляты и нефтепродукты , образующиеся при различных процессах переработки нефти, тоже используют как исходное сырье в нефтехимических процессах, точнее как источник для выделения тех или иных групп углеводородов. Так, из продуктов каталитического риформинга выделяют ароматические углеводороды, из продуктов термического и каталитического крекинга - олефины, из продуктов депарафинизации дизельного топлива – парафины.
Углеводороды, выделяемые из углеводородного сырья, имеют большое практическое значение. Например, метан природного газа используют как топливо и сырье для получения водорода, ацетилена, аммиака и метанола. Этан служит сырьем для процессов пиролиза с целью получения этилена; газовые конденсаты – сырьем для получения бутадиена, изопрена, ароматических углеводородов.
v Требования к углеводородному сырью
К углеводородному сырью для нефтехимических процессов обычно предъявляют значительно более жесткие требования, чем к сырью для процессов переработки нефти.
Реакции, используемые в нефтехимическом синтезе, большей частью каталитические или радикально-цепные, причем для получения требуемых продуктов необходима высокая селективность катализатора, совершенно недопустимы побочные реакции и т.д. Поэтому требуется высокая степень чистоты сырья. Так, для производства этилового спирта прямой гидратацией этилена требуется 97-98%-ный этилен, практически свободный от сероводорода (до 0,002 % Н 2 S). Для производства полиэтилена высокого давления требуется 99,99%-ный этилен, совершенно свободный от ацетилена.
Тщательная очистка от сероводорода этилена при получении этилового спирта необходима потому, что ректификационная аппаратура для выделения получаемого спирта из реакционной смеси быстро корродирует и выходит из строя. По этой же причине этилен не должен содержать ацетилена.
При окислении жидких и твердых парафинов до спиртов и кислот необходимо, чтобы в исходном сырье содержалось минимальное количество (до 0,5%) нафтеновых и ароматических углеводородов, тормозящих окисление. Не менее важно отсутствие фенолов, азотистых и сернистых соединений, обрывающих цепь окисления. В связи с этим требования по содержанию серы в ароматических углеводородах являются жесткими (не более 0,02%) и допустимое ее содержание постоянно понижается.
В ряде случаев необходима очистка углеводородного сырья от изомеров и гомологов той же химической природы. Так, если в парафинах имеются углеводороды изостроения, продукты последующего окисления содержат повышенное количество низкомолекулярных кислот, а также изокислот с крайне неприятным запахом.
Примесь диенов в олефинах приводит к развитию смолообразования при изомеризации и алкилировании.
Для углеводородного сырья должны быть ограничения по содержанию оксидов углерода, аммиака и по влажности.
Все выше сказанное говорит о необходимости тщательной подготовки углеводородного сырья.
v Значение предварительной подготовки углеводородного сырья к переработке
Углеводородное сырье должно отвечать высоким требованиям, определяемым спецификой дальнейших химических превращений углеводородов. Одно из основных требований к углеводородному сырью – минимальное содержание или полное отсутствие веществ иной химической природы. Тщательная подготовка углеводородного сырья к переработке необходима для того, чтобы не было коррозии технологического оборудования; увеличивался срок службы катализаторов; исключалась забивка трубопроводов и их пропускная способность; уменьшалось количество побочных продуктов, увеличивался выход целевого продукта и повышалось его качество.
Продукты этой отрасли промышленности отличаются большим многообразием строения, свойств и областей применения. Это различные углеводороды, хлор- и фторпроизводные, спирты и фенолы, простые эфиры, альдегиды и кетоны, карбоновые кислоты и их производные (сложные эфиры, ангидриды, нитрилы и др.), амины и нитросоединения, вещества, содержащие серу и фосфор, и т. д. По назначению все они подразделяются на две группы: промежуточные продукты для синтеза других веществ в этой же или других отраслях органической технологии и продукты целевого применения в разных отраслях народного хозяйства.
Промежуточные продукты. Многие вещества, почти не имеющие целевого применения в народном хозяйстве, производят главным образом для того, чтобы на их основе синтезировать другие ценные соединения. Это - промежуточные продукты органического синтеза. Так, основную массу 1,2-дихлорэтана производят для последующей переработки в винилхлорид, окись этилена для получения моноэтиленгликоля.
Роль, масштабы производства и ассортимент промежуточных продуктов очень велики, так как синтез органических соединений протекает через ряд промежуточных стадий.
Мономеры и исходные вещества для полимерных материалов. Их производство занимает одно из самых важных мест в основном органическом и нефтехимическом синтезе, обеспечивающем сырьем промышленность пластических масс, синтетического каучука, синтетических лаков, клеев, пленочных материалов, волокон.
Все синтетические полимеры получают двумя основными способами-полимеризацией и поликонденсацией. Для первой из этих реакций требуются мономеры, т. е. вещества, способные под влиянием тепла, света, облучения или катализаторов соединяться друг с другом без выделения каких-либо низкомолекулярных соединений и давать длинные цепи полимера с теми же элементарными звеньями, как в исходном мономере: полимеризация этилена.
Из мономеров отметим моноолефины (этилен, пропилен, изобутен), диены (бутадиен-1,3 и изопрен, являющийся основой при получении каучука) и стирол.
При поликонденсации исходные вещества должны иметь не менее двух функциональных групп, способных реагировать друг с другом. Так, при образовании полиэфиров взаимодействуют гидрокси- и карбокси-группы:
Исходные вещества для поликонденсационных процессов принадлежат к разнообразным ди- и полифункциональным соединениям. Это - фосген СОС1 2 , дикарбоновые кислоты, их ангидриды и хлорангидриды, а также ряд поликарбоновых кислот и их ангидридов, гликоли и полигликоли, диамин:

При реакциях полимеризации и поликонденсации очень важное значение имеет чистота реагентов. Содержащиеся в них примеси могут ингибировать реакцию или обрывать рост цепи молекулы при полимеризации, нарушать нужное соотношение исходных веществ при поликонденсации, приводя к полимерам со слишком малой молекулярной массой и пониженными техническими показателями. В этом отношении к продуктам основного органического и нефтехимического синтеза предъявляют очень высокие требования, причем чистота мономеров нередко должна соответствовать содержанию основного вещества 99,8- 99,9 % и более (изобутилен полимеризационной чистоты).
Пластификаторы и другие вспомогательные вещества для по лимерных материалов. В производстве синтетических полимеров и изделий из них наряду с мономерами и исходными веществами большую роль играют пластификаторы и другие вспомогательные вещества, которые способствуют процессу синтеза или улучшают технические свойства получаемых полимеров и изделий.
Пластификаторами (или мягчителями) называют вещества, добавляемые к некоторым полимерам в количестве до 30-40 % для улучшения их пластических, эластических свойств. Это необходимо, во-первых, при переработке полимеров прессованием, вальцеванием и другими методами, для чего полимеры должны быть достаточно текучими. Одной из важнейших групп пластификаторов являются высококипящие сложные эфиры, например дибутил- и диоктилфталаты, некоторые эфиры высших спиртов с дикарбоновыми кислотами или высших карбоновых кислот с двухатомными спиртами, алкилароматические углеводороды, низшие полиолефины и др.
Стабилизаторами называют вещества, повышающие стойкость полимеров и резин к окислительному старению. В качестве стабилизаторов применяются алкилфенолы, ароматические диамины.
Синтетические поверхностно-активные и моющие вещества . Поверхностно-активные свойства появляются у органических веществ, содержащих в молекуле гидрофобную группу и наряду с ней гидрофильную (полярную) группировку, способную к сольватации водой. В обычном мыле - натриевой соли стеариновой или пальмитиновой кислоты RCOONa роль этих групп выполняют соответственно длинная углеводородная цепь и карбоксилатная группа.
Ввиду такой особенности строения поверхностно-активное вещество (ПАВ) концентрируется на поверхности раздела фаз, ориентируясь своей гидрофобной группой к масляно-жировому компоненту системы, а гидрофильной - к воде. В результате значительно уменьшается поверхностное натяжение, что способствует хорошему смачиванию материала и переходу загрязнений в воду. Поверхностно-активные вещества обладают также эмульгирующими и диспергирующими свойствами, пенообразующей способностью.
Поверхностно-активные и моющие вещества особенно широко применяют в быту для стирки тканей и изделий из них и чистки различных предметов. В текстильной промышленности их используют для обработки тканей перед крашением, в машиностроении и металлообработке - при резании металлов, для очистки деталей от масел и механических загрязнений, в парфюмерной промышленности - как компоненты туалетного мыла и косметических средств. В химической технологии они служат эмульгаторами при гетерофазных реакциях (в особенности при эмульсионной полимеризации).
Поверхностно-активные и моющие вещества разделяют на ионогенные и неионогенные, отличающиеся наличием или отсутствием групп, способных к диссоциации в водных растворах. Ионогенные вещества в свою очередь бывают анионо- и катионоактивными, в которых поверхностно-активные свойства определяются соответственно анионом или катионом, образующимся при диссоциации.
К анионоактивным веществам относятся наиболее важные промышленные моющие вещества, в том числе мыла - обычное и получаемое из синтетических жирных кислот (активная часть молекулы - группа RCOO~). Такие ПАВ имеют щелочную реакцию и способствуют разрушению тканей, дают с солями магния и кальция нерастворимые соли, что снижает их моющие свойства в жесткой воде, проявляют активность лишь при значительной концентрации в воде. Эти недостатки в значительной степени отсутствуют у современных синтетических анионоактивных веществ, большинство которых представляют собой натриевые соли органических сульфокислот и кислых эфиров серной кислоты. К их числу принадлежат алкиларенсульфонаты RC 6 H4SO 2 ONa, алкилсульфонаты RSO 2 ONa и алкилсульфаты ROSO 2 ONa с алкильными группами С 12 -C 18 .
Катионоактивные моющие вещества имеют сравнительно небольшое практическое значение. Они чаще всего представляют собой соли аминов или четвертичных аммониевых оснований, например соль алкилбензилтриметиламмония + C1-
В последние годы начали все шире использовать неионогенные моющие вещества. Их синтезируют из этиленоксида и различных органических соединений - алкилфенолов, карбоновых кислот, спиртов, аминов и других веществ с активными атомами водорода. Гидрофильные свойства им придает оксиэтильная цепь, например R(OCH 2 CH 2) n OH.
Поскольку поверхностно-активные вещества после их употребления попадают в сточные воды, важным требованием является высокая степень их биоразлагаемости, т. е. способности к окислению в безвредные вещества под влиянием микроорганизмов, находящихся в естественных водоемах. Это налагает определенные ограничения на строение входящего в состав ПАВ углеводородного остатка, который не должен быть разветвленным.
Синтетическое топливо, смазочные масла и добавки к ним. Многие продукты основного органического и нефтехимического синтеза имеют важное значение в автомобильном транспорте, авиации, ракетной технике и других областях. К ним относятся синтетические моторные и ракетные топлива, смазочные масла, присадки, улучшающие свойства топлив и масел, антифризы, препятствующие замерзанию охлаждающих жидкостей, тормозные и гидравлические жидкости.
В качестве высокооктановых компонентов моторных топлив применяют изопарафины, изопропилбензол С 6 Н 5 СН(СН 3)2, трет-бутилметиловый эфир (СН 3)зСОСН 3 и др.
Синтетические смазочные масла принадлежат к нескольким группам органических соединений, из которых важнейшими являются следующие: синтетические углеводороды (низшие полимеры олефинов и алкилированные ароматические углеводороды); сложные эфиры двухосновных карбоновых кислот и высших одноатомных спиртов, а также высших монокарбоновых кислот и многоатомных спиртов.
Применяют различные присадки, повышающие эксплуатационные качества топлив и масел и их стабильность при хранении. Антиокислительные присадки к топливу и смазочным маслам, а также к полимерам (например, алкилированные фенолы) замедляют цепные реакции автоокисления. Другие присадки понижают температуру застывания масел (депрессоры), улучшают их вязкостные свойства (вязкостные присадки), препятствуют коррозии металлов (ингибиторы коррозии) и т. д.
Растворители и экстрагенты . Синтетические растворители должны, кроме того, был дешевыми, легко доступными и мало токсичными. Температура кипения их не должна быть слишком низка во избежание чрезмерных потерь и не должна быть слишком высока, чтобы их можно было регенерировать путем отгонки. В ряде случаев удалось синтезировать растворители с пониженной пожароопасностью и даже совсем негорючие.
В настоящее время растворители и экстрагенты применяют очень широко: для выделения ароматических углеводородов из продуктов переработки нефти, в процессах азеотропной и экстрактивной перегонки, для извлечения жиров и масел из природных веществ. В химической промышленности их часто используют, например, для очистки и перекристаллизации, как абсорбенты газов и паров (ацетилена и летучих веществ, уносимых газами), при синтезе полимеров (особенно в лакокрасочной промышленности). В машиностроении и металлообработке рас творителями обезжиривают и очищают детали. В сельском хозяйстве растворители нужны при употреблении пестицидов.
Синтетические растворители и экстрагенты могут принадлежать к различным группам органических соединений. Это - бензол, хлорпроизводные углеводородов (тетрахлорметан, дихлорметан, три- и тетрахлорэтилен), спирты (этанол, пропанол, бутанолы, пентанолы), целлозольвы, простые эфиры (диэтиловый, диизо-пропиловый и высшие), кетоны (ацетон, метилэтилкетон, изобутилметилкетон), сложные эфиры (этил-, бутил- и пентилаце-тат), а также диметилформамид HCON(CH 3)2, диметилсульф-оксид (CH 3) 2 SO и др.
Пестициды и химические средства защиты растений . Пестицидами (или ядохимикатами) называют вещества, обладающие токсичными свойствами по отношению к тем или иным живым организмам - от бактерий и грибков до растений и вредных животных. Значительная часть пестицидов применяется в сельском хозяйстве в качестве химических средств защиты растений; кроме того, их используют в быту, для борьбы с распространителями болезней и эпидемий, для уничтожения вредителей на складах, в трюмах кораблей, в жилых зданиях и т. д. Применение пестицидов в сельском хозяйстве позволяет избежать многих болезней полевых и садовых культур и значительно уменьшить потери урожая. В связи с этим химические средства защиты растений стали не менее важным фактором в повышении урожайности, чем химические удобрения.
Органический синтез
Промышленность органического синтеза с каждым годом увеличивает выпуск и ассортимент химических продуктов. Среди них можно указать разнообразные мономеры и на их основе синтетические смолы, каучуки, волокна, пластмассы, клеи, красители и большое количество различных лакокрасочных и смазочных материалов, растворителей, поверхностно-активных веществ, ядохимикатов, флотореагентов, антифризов и антидетонаторов, взрывчатых и лекарственных препаратов, фотореактивов, душистых соединений и т. д.
СЫРЬЕ ОРГАНИЧЕСКОГО СИНТЕЗА
В настоящее время почти весь органический синтез базируется на ископаемом органическом сырье: нефти и природных газах, каменном угле, сланцах. В процессах физико-химических превращений этих веществ (риформинг, конверсия, крекинг, пиролиз, коксование, перегонка и ректификация, абсорбционно-десорбционные методы) получают пять групп исходных веществ, используемых для синтеза многих тысяч других соединений (рис.1):
1) парафиновые углеводороды (от СН 4 до смесей C 15 -C 40);
2) олефины (главным образом С 2 Н 4 , С 3 Н 6 , C 4 H 8);
3) ацетилен;
4) оксид углерода и синтез-газ;
5) ароматические соединения (бензол, толуол, нафталин и др.).
Кроме того, в органической технологии в больших количествах
используют и неорганические соединения: кислоты, щелочи, соду, хлор и т. п., без которых невозможно осуществление многих процессов.
| |
В своем развитии промышленность органического синтеза разделилась на ряд специфичных отраслей, среди которых важное место занимает промышленность основного органического и нефтехимического синтеза. Подобно основной неорганической химии и технологии, термин «основной» органический синтез охватывает производство многотоннажных органических веществ, служащих базой для всей остальной органической технологии.
Главным объектом основного органического синтеза является первичная переработка пяти видов исходных веществ в другие продукты (различные углеводороды, хлорпроизводные, спирты и эфиры, альдегиды и кетоны, карбоновые кислоты и их производные, фенолы, нитросоединения, сероорганические соединения, т. е. вещества, на которых основано получение всех других органических продуктов). По практическому назначению продукты основного органического синтеза подразделяют на промежуточные продукты (полупродукты) для синтеза других веществ и продукты целевого назначения.
Связь исходного сырья с готовым продуктом можно представить схемой:
Исходное сырье ® Полупродукты ® ... ® Готовый продукт
Рассмотрим это на следующем примере. Продукт нефтехимической и коксобензольной промышленности бензол служит хорошим растворителем жиров, смол, каучука, серы и других соединений. В то же время он представляет исходное сырье для получения фенола, стирола, нитробензола, анилина, малеинового ангидрида, моносульфокислоты и других химических продуктов и полупродуктов, используемых для изготовления синтетического каучука, пластмасс, лаков, взрывчатых веществ, фармацевтических препаратов и др.
Тема: Современное состояние нефтехимического синтеза. Основные продукты и технологии
Введение
1. Альтернативные виды топлива, сырьевые ресурсы
1.1 Диметиловый эфир
1.2 Синтетический бензин
1.3 Спиртовые топлива
1.4 Топливо из биомассы
2. Технологии
2.1 Синтез ДМЭ из природного газа (через метанол)
2.2 Одностадийный синтез ДМЭ из синтез-газа и синтез бензина (через ДМЭ)
2.3 Нетрадиционные процессы и технологии получения моторных топлив
2.3.1 Технология БИМТ
2.3.2 Технология БИМТ-2
2.3.3 Процесс БИЦИКЛАР
Заключение
Литература
Введение
На развитие топливной отрасли определяющим образом влияет ряд факторов. Рост затрат на поиск, добычу и доставку к местам массового потребления нефтяного сырья в конечном итоге привел к удорожанию топлива, получаемого из нефти. Повышение требований экологов к качеству производимого моторного топлива также вызывает удорожание переработки исходных нефтяных фракций.
Еще один важный фактор, определяющий траекторию изменений в топливном секторе энергетики, обусловлен необходимостью сокращения выбросов в атмосферу диоксида углерода, являющегося основным "парниковым" газом. С позиций эколога ни один из существующих сейчас видов топлива нельзя считать приемлемым. Все, что используется на транспорте для производства энергии, - это соединения углерода. При их сгорании в двигателе автомобиля или в топке энергоустановки (завода или электростанции) образуется (в оптимальном варианте) диоксид углерода, поступающий в атмосферу. Будущее автомобильного транспорта и крупных энергоустановок, как правило, связывают с использованием электрической энергии и водорода, производимыми на базе возобновляемых источников энергии методами, которые, как сейчас кажется, не нанесут ущерба природе. Осуществление этих амбициозных проектов связано со множеством технических проблем, на решение которых уйдет довольно много времени даже при условии мобилизации глобального научно-технического потенциала.
В настоящее время на фоне удорожания нефти и методов ее переработки, растущей автомобилизации и возрастающей потребности цивилизации в высококачественном топливе химики обращают свое внимание в сторону не нефтяных источников для производства новых композиций углеводородных топлив, ставших привычными для потребителя-автомобилиста.
В настоящее время единственным экономически приемлемым путем повышения экологичности автотранспорта является перевод его на альтернативные топлива, обеспечивающие сокращение вредных выбросов в окружающую среду двигателями автомобилей до уровня, отвечающего жестким европейским нормам. Европейская комиссия планирует разработку масштабной программы внедрения альтернативных видов моторного топлива. До 2020 года свыше 1/5 объема топлива на базе нефти должно быть заменено на такие альтернативные продукты, как биотопливо, природный газ и водород.
1. Альтернативные виды топлива, сырьевые ресурсы
1.1 Диметиловый эфир
Синтез диметилового эфира (ДМЭ) и бензина через диметиловый эфир – одно из новых направлений в области переработки природного газа и других источников углерода (уголь, древесные остатки и т.п.). Основные пути переработки метана в моторные топлива показаны на схеме 1. Как видно из схемы, синтез ДМЭ вписывается в схему переработки природного газа как путь, альтернативный синтезу метанола.
Моторные топлива
Хема 1 Основные пути переработки природного газа в моторные топлива
1.2 Синтетический бензин
Сырьем для производства синтетического ненефтяного бензина могут быть уголь, природный и попутный нефтяной газы, биомасса, сланцы и т.д. Наиболее перспективным источником для производства альтернативных моторных топлив является природный газ, а также получаемый из него синтез-газ (смесь СО и Н2 в различных соотношениях). Там, где природный газ легко извлекается, можно использовать его в сжатом и сжиженном состояниях в качестве моторного топлива для двигателей внутреннего сгорания. Сжижение природного газа по сравнению со сжатием имеет то преимущество, что позволяет уменьшить объем системы его хранения почти в три раза.
Использование альтернативных топлив, полученных из природного газа, обеспечивает снижение содержания токсичных компонентов в выхлопных газах автотранспорта.
1.3 Спиртовые топлива
Существенным недостатком этого вида топлива остается его высокая стоимость – в зависимости от технологии получения спиртовые топлива в 1,8-3,7 раза дороже нефтяных. Среди различных спиртов и их смесей наибольшее распространение в качестве моторного топлива получили метанол и этанол. В настоящее время для производства метанола применяют синтез-газ, но для крупномасштабных процессов более предпочтительным сырьем является природный газ. С энергетической точки зрения достоинство спиртов заключается главным образом в их высокой детонационной стойкости, что определяет преимущественное использование спиртов в двигателях внутреннего сгорания с искровым зажиганием. Их основными недостатками являются пониженная теплота сгорания, высокая теплота испарения и низкое давление насыщенных паров.
Этанол в целом по эксплуатационным характеристикам лучше метанола. Стоимость этанола в среднем гораздо выше себестоимости бензина. В настоящее время метанол как моторное топливо используется в ограниченных количествах. Его в основном применяют для получения синтетических жидких топлив, в качестве высокооктановой добавки к топливу и как сырье для производства антидетонационной добавки – метил-трет-бутилового эфира.
Одной из наиболее серьезных проблем, затрудняющих применение добавок метанола, является низкая стабильность бензино-метанольных смесей и чувствительность их к присутствию воды. Различие плотностей бензина и метанола и высокая растворимость последнего в воде приводят к тому, что попадание даже небольших количеств воды в смесь вызывает ее немедленное расслоение, причем склонность к расслоению усиливается с понижением температуры, увеличением концентрации воды и уменьшением содержания ароматических соединений в бензине. Для стабилизации бензино-метанольных смесей используют присадки – пропанол, изопропанол, изобутанол и другие спирты.
1.4 Топливо из биомассы
Весьма перспективным возобновляемым сырьем является биомасса. Она может быть использована для получения этанола в качестве альтернативного топлива. Подсчитано, что ежегодно выращивается и вырастает в дикой природе столько биомассы, что из нее можно вырабатывать энергии в восемь раз больше, чем в настоящее время дает все топливо из ископаемого сырья. Исследования, направленные на создание производства жидких топлив из возобновляемого сырья растительного происхождения, в последние годы расширяются.
Биоэтанол и биобутанол получают ферментационным путем. В качестве сырья для ферментации может быть использован широкий набор углеводных материалов: сахара, крахмал, целлюлоза и др. Основу производства биоэтанола из крахмала составляют две стадии: гидролиз крахмала до глюкозы под действием ферментов и ферментация глюкозы до этанола. Существенный недостаток этой технологии связан с тем, что при повышении концентрации этанола в реакционной смеси выше определенного уровня он начинает оказывать ингибирующее действие на процесс ферментации. Кроме того, ферментация обычно приводит к образованию ряда метаболитов, которые при повышенных концентрациях также снижают эффективность процесса.
Современные исследования по совершенствованию существующих процессов получения биоэтанола ведутся в основном по двум направлениям: разработка ферментационных систем, работающих в непрерывном режиме, и повышение производительности методов извлечения и очистки этанола с целью снижения энергозатрат на производство топливного спирта.
2. Технологии
2.1 Синтез диметилового эфира из природного газа (через метанол)
Природный газ является наиболее простым и доступным сырьем для синтеза диметилового эфира и, соответственно, процесс получения ДМЭ на базе природного газа имеет наилучшие экономические показатели. В настоящее время промышленное производство ДМЭ (наполнитель для аэрозолей) составляет ок. 150 тыс. т. в год и базируется на переработке метанола. Упрощенно схему производства ДМЭ на основе природного газа через синтез и последующую дегидратацию метанола можно представить в виде схемы 2.
Схема 2 Схема синтеза ДМЭ из природного газа через стадии синтеза и дегидратации метанола
Рассмотрим отдельные стадии этого синтеза.
Конверсия метана.
Конверсия метана (риформинг) в синтез-газ – это высокотемпературный процесс, который может быть осуществлен по разным реакциям (с участием различных реагентов). Среди них:
паровая конверсия CH4+H3O=CO+3H3 (1)
углекислотная конверсия CH4+CO2+2CO+2H3 (2)
неполное окисление CH4+1/2O2=CO+2H3 (3)
Реакции (1) и (2) сильно эндотермичны, поэтому получил распространение автотермический риформинг – паровой риформинг в присутствии кислорода. К протекающим в условиях автотермического риформинга реакциям (1) и (3) добавляются сильно экзотермические реакции полного окисления:
CH4+2O2=CO2+2H3O (4)
H3+1/2O2=H3O (5)
CO+1/2O2=CO2 (6)
Эти процессы обеспечивают компенсацию потерь тепла в реакции (1), но приводят к дополнительным затратам сырья.
Синтез-газ представляет собой смесь СО и водорода с небольшим количеством СО2, в котором также может присутствовать азот. Важнейшей характеристикой синтез-газа является соотношение концентраций Н2:СО. Для синтеза метанола это отношение должно быть больше двух, что делает неизбежным использование парового риформинга (реакция 1).
Условия проведения риформинга являются результатом компромисса между требованиями термодинамики (повышение температуры и снижение давления для увеличения равновесной конверсии метана), экономики и материаловедения. При высокой температуре (800-900 ºС) и не слишком высокой давлении (1-3 МПа) термодинамика процесса благоприятна, что позволяет довести реакцию до превращения, близкого к полному. Достигнутый компромисс приводит к тому, что в процессе синтеза метанола стадия риформинга требует примерно 2/3 капитальных вложений и более половины эксплуатационных расходов. Это обстоятельство обусловило поиск новых путей превращения природного газа в синтез-газ.
Прямое газофазное селективное окисление метана в СО и Н2, т.е. в синтез-газ (реакция 3), явилось бы наиболее простым из альтернативных методов, однако селективность этого процесса в удобных для практики условиях низка (на уровне 50%). Высокая селективность может быть достигнута при высоких температурах (ок. 1500 К), когда равновесие благоприятно именно для образования синтез-газа. Однако проведение процесса при таких температурах сопряжено с рядом трудностей, обусловленных очень жесткими требованиями к материалу реактора, контактирующего с коррозийно активной средой при высокой температуре, и сложностью управления процессом, поскольку закономерности горения "богатых" смесей относительно мало изучены.
Возникает также вопрос, что использовать в качестве окислителя. Если окислять метан чистым кислородом, возрастают капиталовложения и стоимость синтез-газа, а если использовать воздух, то получается "бедный" синтез-газ низкого качества с большим содержанием азота (не менее 50-60% об.).